Zobacz więcej
20 marca 2008
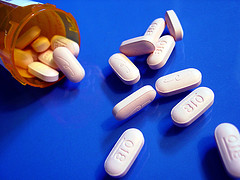
Wybór marki, czy nazwy produktu jest bez wątpliwości jedną z najistotniejszych decyzji w ramach przyjmowanej dla danego produktu strategii marketingowej. W przypadku produktów leczniczych wybór marki wydaje się zadaniem wyjątkowo trudnym.
Zobacz więcej >
Zobacz więcej
Autor: Wojciech L. Olszewski
17 marca 2008
Wojewódzki Sąd Administracyjny wyrokiem z 4 marca 2008 r. (sygn. VII SA/Wa 2179/07) uchylił zaskarżoną decyzję Ministra Zdrowia umarzającą postępowanie w sprawie wydania pozwolenia na obrót produktu biobójczego.
Zobacz więcej >
Zobacz więcej

22 lutego 2008
Guenter Verheugen, Wiceprzewodniczący Komisji Europejskiej podczas przemówienia w Parlamencie Europejskim, ogłosił, że Komisja ma w planach przyspieszenie inicjatywy ustawodawczej w sprawie podróbek leków pojawiających się w imporcie równoległym.
Zobacz więcej >
Zobacz więcej

4 lutego 2008
15 stycznia 2008 roku Komisja Europejska rozpoczęła badanie sektorowe rynku farmaceutycznego. Pierwszym etapem prowadzonego postępowania była seria niezapowiedzianych kontroli w siedzibach firm farmaceutycznych. Badanie sektorowe jest jednym z instrumentów, za pomocą których Komisja Europejska wykonuje swoje traktatowe zadania związane z nadzorem nad prawidłowym funkcjonowaniem mechanizmów konkurencji na rynku europejskim.
Zobacz więcej >
Zobacz więcej

Autor: Agnieszka Deeg
21 stycznia 2008
W dniu 23 sierpnia 2007 r. Sejm Rzeczpospolitej Polskiej uchwalił ustawę o przeciwdziałaniu nieuczciwym praktykom rynkowym (dalej jako „UPNP”), która została opublikowana 20 września 2007r. Na mocy art. 21 UPNP ustawa wchodzi w życie po upływie 3 miesięcy od jej ogłoszenia, to jest dnia 21 grudnia 2007r. Akt ten będzie miał istotne znaczenie dla sektora farmaceutycznego, w szczególności w zakresie marketingu i reklamy.
Zobacz więcej >
Zobacz więcej

Autor: Agnieszka Deeg
8 stycznia 2008
Zgodnie z obowiązującym prawem, sponsor badania klinicznego prowadzonego na terytorium Polski, który nie posiada siedziby na terytorium jednego z państw członkowskich Unii Europejskiej lub państw członkowskich Europejskiego Porozumienia o Wolnym Handlu (EFTA) - strony umowy o Europejskim Obszarze Gospodarczym („EOG”), może działać wyłącznie przez swojego prawnego przedstawiciela posiadającego siedzibę na tym obszarze (art. 2 pkt 37a ustawy z dnia 6 września 2001r. Prawo farmaceutyczne, Dz.U. z 2004r., nr 53, poz. 533; ze zm. – „PF”).
Zobacz więcej >
Zobacz więcej

5 grudnia 2007
Reklamy farmaceutyków z udziałem gwiazd sportu i show-biznesu to już zamknięta historia. Polski ustawodawca ostatecznie wyeliminował błąd w tłumaczeniu słowa „celebrities", jaki popełniono w 2001 r. podczas prac nad dostosowaniem polskiego prawa do unijnej dyrektywy. Dotąd prawo zakazywało reklamy środków leczniczych z udziałem osób pełniących funkcje publiczne, czyli np.: parlamentarzystów, radnych czy pracowników administracji rządowej.
Zobacz więcej >
Zobacz więcej

Autor: Agnieszka Deeg
14 listopada 2007
w załączeniu jesienne wydanie Lifesciences Bulletin, który został przygotowany przez Grupę Farmaceutyczną CMS Cameron McKenna. Enclosed please find the autumn edition of the Lifesciences Bulletin prepared by the Pharmaceutical Team from CMS Cameron McKenna.
Zobacz więcej >
Zobacz więcej

Autor: Agnieszka Deeg
9 listopada 2007
Znowelizowana dnia 24 sierpnia 2007 r. ustawa o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych wprowadza grupę nowych tzw. przepisów antykorupcyjnych (art. 63a-63c) i połączone z nimi przepisy karne (art. 192b-c). Przepisy te budzą uzasadnione wątpliwości warte omówienia.
Zobacz więcej >
Zobacz więcej

9 października 2007
Do przestępstw ustawa zalicza produkcję lub wprowadzanie do obrotu środka spożywczego powszechnie spożywanego szkodliwego dla zdrowia lub życia człowieka (art. 96). W takiej sytuacji ustawodawca przewidział karę grzywny, ograniczenia wolności lub pozbawienia wolności do lat 2. Kara jest ostrzejsza (zagrożenie karą grzywny, ograniczenia wolności albo pozbawienia wolności do lat 3) w przypadku produkcji lub wprowadzania do obrotu szkodliwego dla zdrowia lub życia ludzkiego środka spożywczego specjalnego przeznaczenia żywieniowego, suplementu diety lub nowej żywności.
Zobacz więcej >
Zobacz więcej

5 października 2007
Przed ostrzem konstytucji i prawa wspólnotowego ustawę o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych może uratować racjonalna wykładnia jej przepisów. I taką właśnie proponują radca prawny współpracujący z kancelarią Salans oraz pani adwokat współpracująca z kancelarią Baker & McKenzie Chodzi o nowelizację tej ustawy z 24 sierpnia (DzU nr 166, poz. 1172). W ostatnim czasie pojawiają się liczne sprzeczne głosy dotyczące skutków jej nowych przepisów, a konkretnie art. 63a - 63c art. 192 b - 192c.
Zobacz więcej >
Zobacz więcej

Autor: Agnieszka Deeg
10 września 2007
Wprowadzenie innowacyjnego produktu leczniczego do obrotu poprzedzone jest w zdecydowanej większości przypadków długim i kosztownym procesem wynalazczym, a następnie badawczym. W związku z powyższym, produkty lecznicze są jednymi z najczęściej chronionych w systemie własności intelektualnej. Najważniejszą rolę odgrywają tu patenty, bowiem zapewniają wyłączność czerpania korzyści ze sprzedaży leków. Do 1993 roku nie było możliwości patentowania produktów leczniczych w Polsce oraz innych krajów naszego regionu. Możliwe było jedynie uzyskanie ochrony na poszczególne procesy ich wytwarzania. Dziś, na jeden produkt leczniczy można uzyskać nawet kilkadziesiąt patentów, najważniejsze z nich dotyczą jednak substancji czynnych.
Zobacz więcej >
Zobacz więcej

6 września 2007
Firmy farmaceutyczne nie mogą się spóźnić nawet o jeden dzień ze złożeniem wniosku o przedłużenie pozwolenia na dopuszczenie leku do obrotu Należy zrobić to najpóźniej sześć miesięcy przedupływem ważności dotychczasowego pozwolenia. Jest to termin bezwzględny, nie można go przedłużyć ani przywrócić - orzekł Naczelny Sąd Administracyjny
Zobacz więcej >
Zobacz więcej

Autor: Agnieszka Deeg
31 sierpnia 2007
Chcielibyśmy poinformować Państwa, że Sejm Rzeczpospolitej Polskiej w dniu 24 Sierpnia 2007 r. uchwalił długo dyskutowaną ustawę o zmianie ustawy z dnia 27 sierpnia 2004 roku o świadczeniach zdrowotnych finansowanych ze środków publicznych.
Zobacz więcej >
Zobacz więcej

18 lipca 2007
Mimo licznych głosów zaniepokojenia wynikających z zauważalnego spadku produktywności procesu badań i rozwoju (BiR) przemysł farmaceutyczny wciąż należy do najbardziej innowacyjnych gałęzi światowej gospodarki. Porównanie bezwzględnych nakładów ponoszonych przez firmy farmaceutyczne oraz inne branże, a szczególnie procentowego udziału wydatków na BiR do przychodów, liczby zgłaszanych wniosków patentowych czy choćby liczby nowych produktów, które co roku dopuszczane są do obrotu przez pełniące tu niejako rolę niezależnego arbitra władze regulatorowe, stawia je w pierwszej trójce przedsiębiorstw najbardziej przyczyniających się do postępu technologicznego (Tabela 1 i 2]. Nowe produkty otrzymywane drogą klasycznej syntezji organicznej czy też coraz śmielej poczynającej sobie biotechnologii lub inżynierii...
Zobacz więcej >
Zobacz więcej

Autor: Agnieszka Deeg
24 czerwca 2007
Rozporządzenie pediatryczne Na rynku istnieje wiele leków, które są stosowane u populacji pediatrycznej, tj. dzieci do 18 roku życia, mimo że nie zostały poddane badaniom klinicznym na tej grupie pacjentów, ani nie zostały dopuszczone do obrotu w tym zakresie. Taki stan może rodzić problemy z określeniem prawidłowego dawkowania, odpowiednich postaci i dróg podania oraz zwiększonego ryzyka wystąpienia działań niepożądanych. W związku z powyższym instytucje wspólnotowe zdecydowały się wydać rozporządzenie, a więc akt stosowany bezpośrednio w państwach członkowskich, w sprawie produktów leczniczych stosowanych w pediatrii (Rozporządzenie z dnia 12 grudnia 2006 r. Nr 1901/2006 Parlamentu Europejskiego i Rady).
Zobacz więcej >
Zobacz więcej

19 czerwca 2007
Zachodzące zmiany na rynku farmaceutycznym są m.in. podyktowane rozwojem biotechnologii i nowych metod terapeutycznych oraz postępem w diagnostyce medycznej. Niemały wpływ ma również coraz większy dostęp do opieki medycznej w krajach rozwijających się. Wygasająca ochrona patentowa wielu farmaceutyków wpływa natomiast na szybki wzrost rynku o wiele tańszych leków odtwórczych.
Zobacz więcej >
















